Modelo atómico de Rutherford: ¿Cómo se llama?
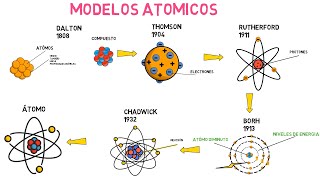

El modelo atómico de Rutherford es uno de los más importantes en la historia de la física y la química. Fue propuesto por el físico neozelandés Ernest Rutherford en 1911, y supuso un gran avance en la comprensión de la estructura de la materia. Este modelo se basa en la idea de que los átomos están compuestos por un núcleo central, que contiene la mayor parte de la masa del átomo, rodeado por electrones que giran alrededor del núcleo. Pero, ¿cómo se llama exactamente este modelo? En este artículo, exploraremos el nombre y las características del modelo atómico de Rutherford.
El modelo atómico de Rutherford: una mirada a su estructura fundamental
El modelo atómico de Rutherford es uno de los más importantes en la historia de la física y la química. Fue propuesto por el físico neozelandés Ernest Rutherford en 1911, y se basa en la idea de que los átomos tienen un núcleo central muy pequeño y denso, rodeado por electrones que giran alrededor de él.
Este modelo fue desarrollado a partir de los experimentos de Rutherford con partículas alfa, en los que se observó que algunas de estas partículas eran desviadas de su trayectoria al atravesar una lámina de oro. Esto llevó a Rutherford a concluir que los átomos no eran una masa uniforme, sino que tenían una estructura interna compleja.
Según el modelo de Rutherford, los electrones giran alrededor del núcleo en órbitas circulares, y la carga positiva del núcleo atrae a los electrones hacia él. Sin embargo, este modelo tenía un problema importante: según las leyes de la física clásica, los electrones deberían perder energía y caer en espiral hacia el núcleo, lo que no se observa en la realidad.
Este problema fue resuelto más tarde por el modelo atómico de Bohr, que propuso que los electrones sólo podían ocupar ciertas órbitas estables alrededor del núcleo, y que sólo podían saltar de una órbita a otra emitiendo o absorbiendo energía en forma de fotones.
A pesar de sus limitaciones, el modelo atómico de Rutherford fue un paso importante en la comprensión de la estructura fundamental de la materia, y sentó las bases para el desarrollo de modelos más complejos y precisos en el futuro.
¿Qué otros modelos atómicos conoces? ¿Cómo han evolucionado a lo largo del tiempo? ¿Qué implicaciones tienen para nuestra comprensión del mundo que nos rodea? Estas son algunas de las preguntas que podemos hacernos al reflexionar sobre el modelo atómico de Rutherford y su legado.
Conoce los modelos atómicos de Thomson y Rutherford: sus características y diferencias
La teoría atómica ha evolucionado a lo largo de la historia, y dos de los modelos más importantes son los de Thomson y Rutherford.
Modelo atómico de Thomson
El modelo atómico de Thomson, también conocido como el modelo del pudín de pasas, fue propuesto en 1904. Según esta teoría, el átomo estaba compuesto por una esfera de carga positiva en la que se encontraban incrustados los electrones, que eran partículas con carga negativa. De esta forma, el átomo era una especie de pudín en el que los electrones se movían libremente.
Modelo atómico de Rutherford
El modelo atómico de Rutherford, propuesto en 1911, fue una evolución del modelo de Thomson. Según esta teoría, el átomo estaba compuesto por un núcleo central muy pequeño y denso, con carga positiva, en el que se encontraban los protones. Los electrones, por su parte, se encontraban en órbita alrededor del núcleo. Este modelo explicaba la existencia de partículas alfa y beta, y permitía entender la radiactividad.
Diferencias entre los modelos
La principal diferencia entre los modelos de Thomson y Rutherford es la estructura del átomo. Mientras que en el modelo de Thomson el átomo era una esfera de carga positiva con electrones incrustados, en el modelo de Rutherford el átomo tenía un núcleo central con protones y electrones en órbita alrededor de él.
Otra diferencia importante es que el modelo de Rutherford permitía explicar la radiactividad, algo que el modelo de Thomson no podía hacer.
Reflexión
La evolución de la teoría atómica es un ejemplo de cómo la ciencia avanza a través de la observación, la experimentación y la reflexión. A medida que se descubren nuevas evidencias, los modelos teóricos se van ajustando y mejorando. Hoy en día, sabemos que el modelo atómico de Rutherford es solo una parte de la teoría atómica, y que existen otros modelos más complejos que nos permiten entender mejor la estructura de la materia.
Explorando el modelo atómico planetario: una mirada a la estructura de los átomos
El modelo atómico planetario es una teoría que describe la estructura de los átomos. Según esta teoría, los electrones giran alrededor del núcleo en órbitas circulares, al igual que los planetas giran alrededor del sol. El núcleo está compuesto por protones y neutrones, y los electrones tienen carga negativa.
Este modelo fue propuesto por Niels Bohr en 1913 y fue una mejora del modelo atómico de Rutherford. El modelo planetario permitió explicar la estabilidad de los átomos y la emisión de luz por parte de los elementos químicos.
El modelo atómico planetario ha sido superado por modelos más complejos, como el modelo cuántico, que tiene en cuenta la dualidad onda-partícula de los electrones y la incertidumbre en la posición de los mismos. Sin embargo, el modelo planetario sigue siendo útil para entender la estructura básica de los átomos.
La exploración de la estructura de los átomos es un tema fascinante y en constante evolución. A medida que se descubren nuevas propiedades y se desarrollan nuevos modelos, nuestra comprensión de la materia y el universo se expande. ¿Qué nuevos descubrimientos nos deparará el futuro en este campo?
El modelo atómico de Rutherford: el experimento que revolucionó la comprensión de la estructura atómica
El modelo atómico de Rutherford es uno de los hitos más importantes en la historia de la física. Fue el resultado de un experimento que revolucionó la comprensión de la estructura atómica. En este experimento, Rutherford bombardeó una lámina de oro con partículas alfa y observó cómo se dispersaban.
Lo que Rutherford descubrió fue que la mayoría de las partículas alfa pasaban a través de la lámina sin ser desviadas, pero algunas eran desviadas en ángulos muy grandes. Esto llevó a Rutherford a concluir que la mayor parte del átomo era espacio vacío, pero que había una pequeña región central densa y cargada positivamente que desviaba las partículas alfa.
Este descubrimiento fue revolucionario porque contradecía el modelo atómico previo, propuesto por Thomson, que afirmaba que el átomo era una esfera uniforme de carga positiva con electrones incrustados en ella. El modelo de Rutherford, por otro lado, sugería que el átomo tenía una estructura más compleja, con un núcleo central cargado positivamente y electrones orbitando alrededor.
El modelo de Rutherford sentó las bases para el desarrollo posterior de la física nuclear y la comprensión de la energía nuclear. También fue un paso importante en la comprensión de la estructura de la materia y la naturaleza de las fuerzas fundamentales.
¿Qué otros experimentos o descubrimientos científicos han cambiado nuestra comprensión del mundo? ¿Cómo podemos seguir avanzando en nuestra comprensión de la naturaleza y el universo?
¡Gracias por leernos!
Si quieres ver otros artículos similares a Modelo atómico de Rutherford: ¿Cómo se llama? puedes visitar la categoría Ciencia o revisar los siguientes artículos
